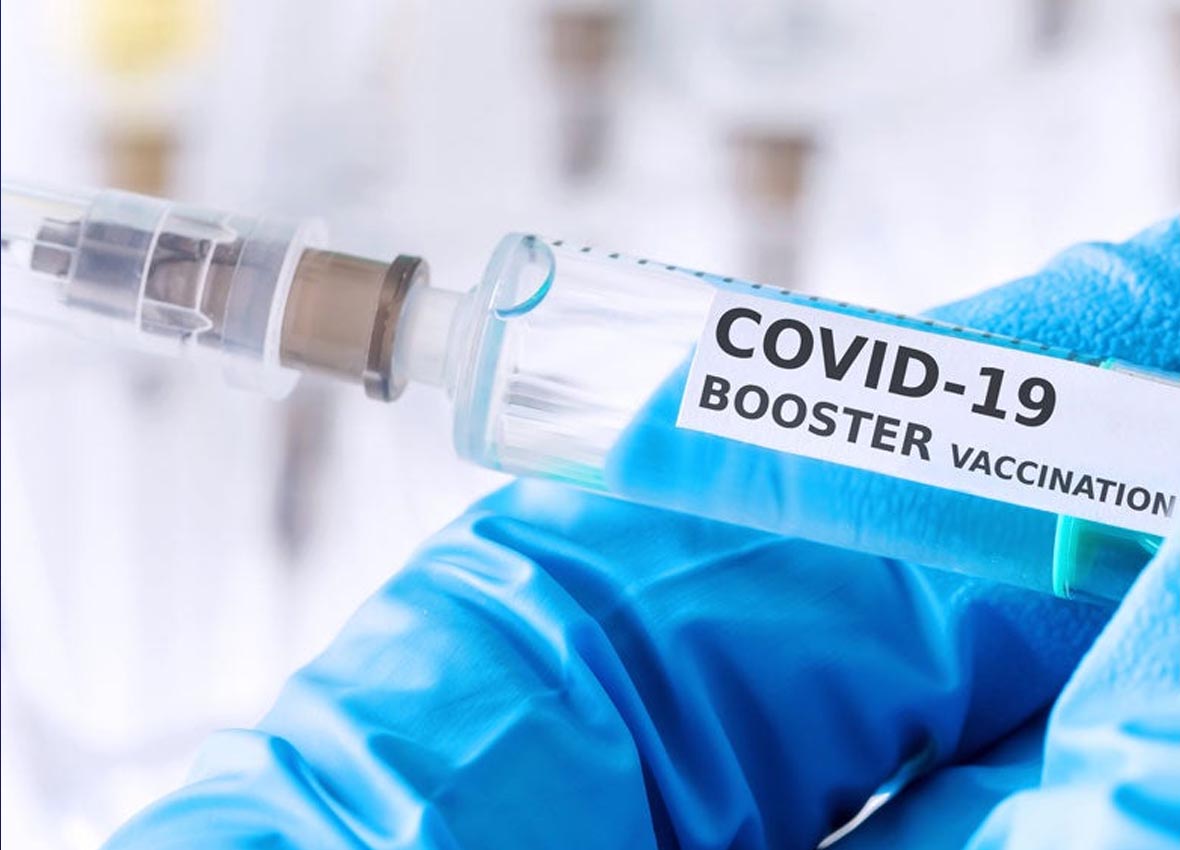
NATANGGAP na ng Food and Drugs Administration (FDA) ang mga aplikasyon ng Pfizer, AstraZeneca, Sinovac, at Sputnik V na humihiling na maamiyendahan ang emergency use authorizations (EUA) ng kanilang mga COVID-19 vaccines at maisama ang booster shot at third dose sa kanilang regimen.
Ayon kay FDA Director General Eric Domingo, natanggap nila ang aplikasyon ng mga naturang kumpanya bago mag-Undas.
Aniya, nais ng mga ito na maisama ang ikatlong dose o booster dose sa kanilang regimen.
Kasama rin aniya sa ipinadala ng mga ito ang kanilang scientific data na siyang pinag-aaralan na ngayon ng ating mga eksperto.
Sinabi ni Domingo na kabilang sa pinag-aaralan nila ay ang bisa ng booster shots.
Ina-assess na rin ng Department of Health (DOH) ang posibleng pagmi-mix and match ng mga bakuna.
“Sa ngayon po ang FDA nakatanggap na po kami nitong bago mag-Undas ng applications for product variations o modification po, amendment ng EUA, galing po sa Pfizer, sa AstraZeneca, sa Sinovac at saka sa Sputnik,” ani Domingo, sa pre-recorded public address kay President Rodrigo Duterte.
“Nag-request po sila na ma-include ang third dose sa kanilang regimen o ang booster dose at pinadala po nila ‘yung kanilang scientific data available at ito po ‘yung inaaral ngayon ng ating mga experts,” ani Domingo.
Una nang sinabi ni DOH Undersecretary Maria Rosario Vergeire na bago makapagbigay ng third dose o booster shot ang pamahalaan ay kailangan munang maamiyendahan ang EUA ng mga bakuna.
Paglilinaw naman ni Domingo, hindi lahat ng tao ay kinakailangan ng COVID-19 booster shots o third dose.
“Ang nakikita rin naman natin na magiging trend ay hindi lahat kakailanganin ng third dose kung hindi talagang ‘yun pong selected na mangangailangan, the elderly, the immunocompromised and healthcare workers,” paliwanag niya.
Inaantabayanan na rin aniya ng pamahalaan ang rekomendasyon ng World Health Organization (WHO) hinggil dito. ANA ROSARIO HERNANDEZ